EL HIPOCLORITO SÓDICO COMO DESINFECTANTE. ¿Cuánto tiempo dura la actividad de una disolución de lejía?
EL HIPOCLORITO SÓDICO
COMO DESINFECTANTE.
Actualizado 23/04/2020
Jefe de dotación de bomberos CPEIS Toledo. Licenciado
en bioquímica por la UCM.
En este artículo voy a explicar cuáles son las características del
hipoclorito sódico y su poder como desinfectante, desmintiendo algunos bulos e
indicando como realizar sencillos cálculos para poder preparar
disoluciones de cualquier concentración.
El hipoclorito sódico cuando tiene carácter comercial se denomina
lejía. Esta forma del hipoclorito está regulada por Real Decreto 349/1993, de 5
de marzo, por el que se modifica la Reglamentación Técnico-Sanitaria de Lejías
aprobada por el Real Decreto 3360/1983, de 30 de noviembre. De este documento
de deriva su definición:
- Lejía: es aquella cuyo contenido en cloro activo no es inferior
a 35 gramos por litro ni superior a 60 gramos por litro y tiene una
alcalinidad total máxima, expresada en óxido de sodio (ONa2), del 0,9
por 100 en peso.
. Lejía concentrada: es aquella cuyo contenido en cloro activo no es
inferior a 60 gramos por litro ni superior a 100 gramos por litro y
tiene una alcalinidad total máxima, expresada en óxido de sodio (ONa2),
del 1,8 por 100 en peso.
Cuando la concentración es mayor a 100 gramos por litro se denomina hipoclorito
industrial.
Características químicas
El hipoclorito sódico se presenta
en diferentes formas en estado sólido, en todos ellas es inestable, por ello la
forma más frecuente de utilización es en disolución acuosa. Esta disolución tienen
un ligero color amarillo y olor a cloro. Presenta carácter básico pH y tanto
mayor cuanto mayor es la concentración ( 5% tiene pH=10; 6,5% pH= 12).
( 6) El
hipoclorito sódico en disolución se disocia según los siguientes equilibrios
químicos:
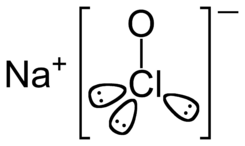
NaClO + H2O ⇄ HClO + Na+ + OH- y HClO ⇄ ClO - + H+
Esta
disociación proporciona al medio dos formas cloradas con capacidad de acción
desinfectante, el ácido hipocloroso (HClO ) y el ión hipoclorito ( ClO -
) . La suma de ambos es lo que se denomina cloro libre.
Si esta disolución se
preparará con agua destilada, el cloro total presente en la disolución sería el
cloro libre pero como en nuestro caso las disoluciones se prepararán con agua
corriente ( no destilada), potable o no potable, existirá una parte del cloro
que reaccionará con materias presentes en el agua como materia orgánica (
derivados aminos) u otros compuestos inorgánicos ( cationes de metales, ácido sulfhídrico,
etc) por lo que una parte del cloro libre se pierde en estas reacciones
disminuyendo el poder desinfectante. A esta fracción de cloro se la denomina
cloro combinado.
A la hora de
preparar un disolución de una concentración concreta para ser usada como
desinfectante ( de 500 a 5.000 ppm o superior) este factor apenas es
significativo salvo en aguas duras (con elevada concentración de sales de
calcio o magnesio) y/o alcalinas (con carbonatos
bicarbonato e hidróxidos), donde sí podría afectar. Sí resulta importante en la
cloración de aguas para consumo o para uso recreativo ( se usan valores de 0,6
ppm).
Características como desinfectante.
Ya en el siglo XVII se comenzó a
reconocer y utilizar como un efectivo bactericida. Posteriormente se fue
estudiando de forma experimental y se le ha ubicado como un desinfectante de
nivel medio-alto en función de la concentración utilizada.
Si bien el mecanismo de actuación
(1)(8) no
está claramente identificado, en diferentes estudios se ha comprobado que el
poder oxidante del hipoclorito en forma de cloro libre interviene en diferente procesos celulares
inactivando o destruyendo microorganismos. La inactivación por cloro
puede ser el resultado de varios factores: oxidación de enzimas sulfhidrilo y
aminoácidos; cloración en anillo de aminoácidos; pérdida de contenido
intracelular; disminución de la absorción de nutrientes inhibición de la síntesis
de proteínas; disminución de la absorción de oxígeno; oxidación de componentes
respiratorios; disminución de la producción de adenosina trifosfato; roturas en
el ADN y ARN; y síntesis de ADN deprimida.
El mecanismo microbicida real del
cloro podría implicar una combinación de estos factores.
El hipoclorito sódico se comporta
como un desinfectante de alto nivel al 0,1%, 1.000 ppm de cloro disponible, con
un tiempo de contacto de diez minutos, y es esporicida al 0,5%, 5.000 ppm, con
un tiempo de contacto de cinco minutos.
En la "Guía técnica para la evaluación y prevención de los riesgos
relacionados con la exposición a agentes biológicos" del Instituto Nacional de Seguridad y Salud en el Trabajo ( INSST), se recogen los datos de
concentración y tiempo del hipoclorito sódico con desinfectante.Tabla siguiente.
Porqué la cantidad de cloro libre coincide con la riqueza de la
disolución. (2) (6)
La riqueza o concentración de una
solución de hipoclorito se expresa tanto en función del contenido de soluto,
como del contenido de cloro activo ya sea en gramos por litro o en %.
El cloro activo de un producto
que nos da la medida del poder oxidante expresada como cloro. Para el caso del
hipoclorito sódico, según su estequiometría y como se observa en las reacciones anteriores se puede por tanto decir que una cantidad de cloro puro,
en solución acuosa, tiene el mismo poder oxidante que una cantidad determinada
de hipoclorito. Como se observa en las reacciones anteriores.
Para calcular la cantidad de
Siendo Volumen de agua que queremos preparar de disolución para la desinfección. Si utilizamos uno recipiente con capacidad de 5.000 litros pero solo
la llenamos a la mitad, nuestro volumen será esa mitad de agua ( 2.500 litros)
Partes por
millón (ppm necesarias ): La dosis del desinfectante
que necesitamos en el agua para la desinfección
%
hipoclorito: Concentración de cloro
libre o gr/litros contenida en el producto. Es necesario revisar en la etiqueta
del producto el % de cloro que contiene o en su defecto consultarlo con su
proveedor.
Factor de
dilución: este valor representa el numero que necesitamos dividir para obtener
la partes por millon, por lo tanto se mantiene siempre igual en 10.000
El contenido o peso de hipoclorito sódico en gr/l de una solución de este, se calcula convirtiendo los gr/l de cloro activo en su equivalente como hipoclorito sódico, para ello basta con multiplicar por la relación de sus respectivos peso moleculares (74 / 71 = 1,05):
gr/l
de hipoclorito sódico = gr/l de cloro útil x 1,05
Ejemplos:
- Venta al
público: (blanqueador casero, comercial): 5% (50 g/l; 50.000 ppm) de cloro libre
- Para limpieza
general, desinfección de mano y ropa: 0,05% (500 mg/L; 500 ppm) cloro libre
- Para
desinfección general de áreas sin materia orgánica: 0,5% (5g/l ; 5.000 ppm)
- Para
desinfección con material orgánico o derrames: 1 % (10 g/l; 10.000 ppm)
Degradación del hipoclorito sódico.
La degradación de hipoclorito
sódico es un hecho conocido desde que se comenzó su utilización. El Real
Decreto 349/1993, de 5 de marzo, por el que se modifica la Reglamentación
Técnico-Sanitaria de Lejías aprobada por el Real Decreto 3360/1983, recoge como
medida para evitar dicho efecto en las lejías, y con el objeto de evitar
los fenómenos de degradación de su contenido en cloro activo previsible en
estos productos, se aceptará una tolerancia de ‒7 y +10 por 100 para las
concentraciones comprendidas entre 35 y 60 gramos de claro activo por
litro y de ±10 por 100 para las comprendidas entre 60 y 100 gramos de
cloro activo por litro.
El hipoclorito sódico es inestable, va perdiendo
cloro a un ritmo mensual del 2 al 4%, perdiendo aún más si la temperatura es
mayor de 30°C. (2)
En los gráficos siguientes se muestra la degradación en función del
tiempo y la temperatura.

Lo que demuestran estos gráficos es el descenso del cloro activo en disoluciones expuestas al aire, a presión atmosférica, en función de la temperatura, llegando a descensos del 50% a 30°C en concentraciones elevadas.
Por otro lado, también se observa
como la concentración de la disolución es otro factor determinante ya que el
porcentaje de pérdida de cloro libre disminuye del 10% en disoluciones de 100
g/l frente al 30% en disoluciones con concentración de 160 g/l.
El calor, la luz, el contacto con
ácidos y ciertos metales, descomponen estas disoluciones en cloro gas, ácido
hipocloroso y ácido clorhídrico. En la descomposición se dan las siguientes
reacciones :
2 NaClO ⇄ 2 NaCl + O2 y 3 NaClO ⇄ 2 NaCl + NaClO3
Los estudios realizados sobre los
efectos de la luz y del pH han demostrado como afectan a la estabilización de
estas disoluciones. (3)
Calculo de disoluciones.
Para calcular las cantidades
necesarias de hipoclorito sódico en disolución a un determinado porcentaje se
utiliza la formula V1= (V2x C2) / C1 donde :
V1= volumen
de hipoclorito necesario al % inicial para
prepara la disolución requerida
V2= volumen
de la disolución final
C1=
concentración de la disolución que disponemos
C2= concentración
de la disolución que queremos preparar
Si partimos de
una disolución de hipoclorito sódico al 4,5% y queremos calcular el agua
necesaria que debo añadir para obtener una disolución de un litro al 0,5%.
V1= ( 1000 x 0.5)
/ 4,5 = 111,1 ml de hipoclorito al 4,5%
el resto será agua hasta completar el litro
final de disolución.
En la Guía de
descontaminación publicada en este blog, en su Anexo 7 se presentan más formas
de cálculo tanto con disoluciones como con agentes sólidos así como una serie
de tablas donde obtener los datos de volúmenes necesario de hipoclorito a diferentes
concentraciones para preparar disoluciones de hasta 12.000 litros.
Conclusiones:
El hipoclorito sódico según la concentración
se puede comportar como desinfectante de alto nivel aunque no es efectivo
frente a priones (1). ( Ver entrada de este blog "Descontaminación de superficies y espacios afectados por el SARS-COV-2") .
Es más efectivo a pH 6 (6).
Es más efectivo a pH 6 (6).
Es inestable a presión atmosférica
al efecto de la luz y del pH , pero el tiempo que dura una disolución a presión
dentro de un pulverizador puede llegar a superar un mes. Hay estudios de
estabilidad que demuestran que soluciones de entre 1.000 ppm, dilución 1:50 de
lejía al 5%, y 10.000 ppm, dilución 1:5 de la lejía al 5%, son estables durante
treinta días si se conservan en envases opacos y bien cerrados (7).
Por lo tanto, no es necesario
preparar diariamente las disoluciones de
lejía.
Referencias:
(1) Guía de uso de desinfectantes en
el ámbito sanitario. Sociedad
española de medicina preventiva, salud pública e higiene..2019
(2) Tratamiento de desinfeccion de
agua potable. Francisco
Ramírez Quirós. Editorial Canal Educa. Canal de Isabel
(3) Estabilidad de la solución de
hipoclorito generado por electrólisis. Ricardo Rojas Vargas, Sixto Guevara Vásquez XXVII Congresso
Interamericano de Engenharia Sanitária e Ambiental. XXVII Congresso
Interamericano de Engenharia Sanitária e Ambiental. ABES - Associação
Brasileira de Engenharia Sanitária e Ambiental.
(4) Ficha de seguridad química del
hipoclorito sódico al 13%. Químicas Meroño. https://www.ecosmep.com/cabecera/upload/fichas/6117.pdf
(5) Guía de hipoclorito sódico. Instituto de hidrología, meteorología y estudios ambientales.
Ministerio de ambiente y desarrollo sostenible de Colombia. http://documentacion.ideam.gov.co/openbiblio/bvirtual/018903/Links/Guia18.pdf
(6) Guía de descontaminación en
intervenciones con riesgo químico, biológico y/o radiológico. E.
Martínez, M. Martínez, J González
(7) Stability and bactericidal
activity of chlorine solutions. Rutala WA1, Cole EC, Thomann CA, Weber DJ.
Infect Control Hosp Epidemiol. 1998
May;19(5):323-7. NCBI. US National Library of Medicine National
Institutes of Health. https://www.ncbi.nlm.nih.gov/pubmed/9613692
(8) Guideline for Disinfection and
Sterilization in Healthcare Facilities, 2008. Update: May 2019. William A. Rutala,
Ph.D., M.P.H.1,2, David J. Weber, M.D., M.P.H.1,2, and the Healthcare Infection
Control Practices Advisory Committee (HICPAC) https://www.cdc.gov/infectioncontrol/guidelines/disinfection/
Guideline for Disinfection










Un artículo buenísimo para todos los que estamos en primera línea. En el se resume lo importante y esencial para saber trabajar con las lejías y sus disoluciones, gracias Fran
ResponderEliminarGracias. Un saludo.
Eliminar